جزوه تایپ شده انتقال جرم و حرارت
دانشگاه پیام نور پارسه علمی کاربردی کارشناسی ارشد دانشگاه آزاد سراسری دکتر ارجمند دکتر غلامسن اسدی دانشگاه صنعتی شریف مهندسی پلیمر
:
:
) (:
//: :
))( *““ ):(
:
( ( ( ) : ))+(( انتقال حرارت:
به صورت تماس با ماده غذایی می باشد و در هدایت Conduction 1(هرسه فاز مایع گاز و جامد صورت می پذیرد. جابجایی یا همرفت Convection 2(
)3 Radiation تابش
فقط در مایعات و گازها است.
هرچه اختلاف چگالی بیشتر باشد ، انتقال بهتر است.
اختلاف چگالی در سیال باعث نیروی شناوری شده و باعث تبادل گرما می شود .)سیالات سرد و گرم ، سیالات سبک و سنگین )بویانسی((.
انتقال انرژی در اثر امواج الکترومغناطیس انجام می شود.
در تمامی فاز ها و حتی خلاء هم قابل انجام است.
هر جسمی که دمای آن از صفر مطلق) 273.15-( بالاتر باشد از خود امواج الکترو مغناطیس ساطع می کند.
در صفر مطلق مولکولها جنبشی ندارند و واکنشی انجام نمی شود.
:)K( Thermal Conductivity قابلیت هدایت حرارتی
معیاری از توانایی یک ماده در رسانش گرما در قیاس با ذخیره انرژی گرمایی در آن ماده است .
K در فلزات زیاد ولی در چوب کم است.
K آب = 6.0 و در مواد غذایی کمتر از 6.0 است.
قانون آرنیوس )رابطه ثابت سرعت واکنش با دما(:
Ea : انرژی اکتیواسیون Ea
اگر در یک جسم یا سیستم گرما تولید شود ‘+q و چنانچه گرما مصرف شود ‘q- در موازنه گرما لحاظ می شود.
به طور کلی در طی فرآیند ها ممکن است واکنش های گرماگیر) Endothermic( یا گرمازا )exothermic( روی دهد که در چنین مواردی ‘q در موازنه لحاظ می شود.
زمانی که می خواهیم موازنه گرما برای یک انبار یا سیلوی حاوی محصولات کشاورزی )گندم ، سیب زمینی ، چغندر و ….( بنویسیم در اثر تنفس گرما تولید می شود که باید در معادله لحاظ شود و یا جهت محاسبات حرارتی در یک سالن تولید ، سردخانه ، حتما باید گرمای ناشی از فعالیت پرسنل و … در نظر گرفته شود.
در جسم یا سیستمی که انتقال حرارت به صورت پایا انجام می شود ، دما در نقاط مختلف جسم یا سیستم فقط تابعی از موقعیت نقاط مورد نظر در جسم می باشد T=F(location) بنابراین در انتقال حرارت به صورت پایا ، دمای نقاط مختلف جسم با هم متفاوت است ولی با گذشت زمان تغییری نمی کند.
در انتقال حرارت ناپایا یا گذرا ، دمای نقاط جزوه انتقال جرم و حرارت جسم علاوه بر تابع موقعیت ، تابع زمان نیز می
. T=F(location, time) باشد
44/70/22
انتقال حرارت به روش هدایت در شرایط پایا در یک دیواره یا تیغه یا جسم لایه ای شکل)Slab(
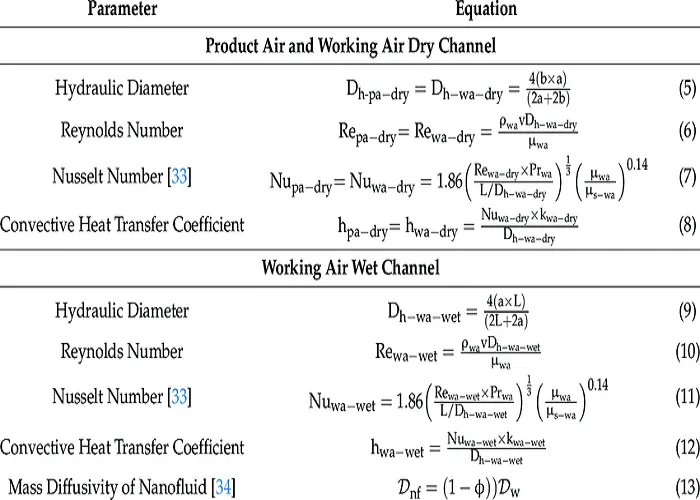
انتقال جرم
نسبت سرعت انتقال حرارت به سطح انتقال را شار می گویند ، به طور کلی نسبت سرعت یک پدیده انتقال
)حرارت یا جرم( به سطح انتقال را شار می گویند .
2
در این رابطه به دلیل اینکه q’x یک بار به A تقسیم شده در نتیجه A در رابطه نهایی نیست.
انتقال حرارت به روش هدایت در شرایط پایا در استوانه تو خالی یا لوله یا Pipe :
فرض کنیم یک سیال داخل یک استوانه توخالی جریان دارد و دمای سطح داخلی لوله به 1T رسیده است و اگر دمای سطح خارجی لوله 2T باشد ، گرما از سطح داخلی به روش هدایت به سطح خارجی منتقل می شود .
T1>T2
گرما توسط مولکول ها از سمت 1r در اثر گرم شدن به مولکول های لایه بعدی منتقل می شود و لایه لایه به سمت بیرون حرکت می کند.
چون دما در سطح داخلی 1T بیشتر از 2T در سطح خارجی است پس گرما از داخل به خارج منتقل می شود.
سطح تبادل حرارت در این حالت از 1A )سطح داخلی لوله( تا 2A )سطح خارجی لوله( متغیر است .بنابراین باید بین 1A و 2A میانگین گرفته شود که میانگین مناسب برای این محاسبات ، میانگین لگاریتمی است.
انتقال حرارت به صورت ناپایا در یک دیواره یا Slab : )در یک بعد مثل x(
در شکل ، یک جزء یا المانی به اندازه dx در نظر می جزوه انتقال جرم و حرارت و برای آن به عنوان یک سیستم موازنه گرما
اطلاعات قبلی
حجم اِِلمان (1) با توجه به شکل
تمامی فرمول ها در صفحه بعد
از روی معادله :
انتقال حرارت در شرایط ناپایا در یک جسم لایه ای شکل با رابطه صفحه قبل تفسیر می شود و طبق رابطه ، دما تابعی از زمان و x است . T= f(x,t)
این معادله دیفرانسیلی بدست آمده برای تجزیه و تحلیل انتقال حرارت در مواد غذایی به شکل لایه ای یا Slab کاربرد دارد )مانند : برگر ، استیک که روی یک سطح گرم قرار می دهیم ( . البته بایستی شرایط مرزی و اولیه برای هر مسئله فیزیکی ، تعیین شود ، همچنین نحوه تماس محصول با واسطه باید لحاظ گردد.
در نهایت برای اینکه این معادلات دیفرانسیلی قابل استفاده شوند، با توجه به شرایط مرزی و اولیه و دامنه تغییرات عدد بیوت Biot حل می شوند و به معادلات جبری قابل استفاده تبدیل می شوند.
این معادلات جبری معمولا به جزوه انتقال جرم و حرارت سری )مجموعه( هستند یعنی دارای ∑ هستند و ممکن است توابع مثلثاتی در آنها وجود داشته باشد.
با استفاده از این معادلات جبری می توانیم پرفایل دما در بعد های مختلف)در اینجا بعد x بود( و همچنین بیشینه دمایی را در محصول بدست آوریم که در مرحله بعد از این پروفایل ها برای تجزیه وتحلیل ،فرآیند هایی که با انتقال حرارت مرتبط هستند استفاده می شود.
معادله انتقال حرارت ناپایا برای یک جسم 3 بعدی:
اگر یک مکعب کوچک از نمونه را انتخاب کنیم یک جسم 3 بعدی ایجاد می شود که فرمول آن به صورت
ی که در انتقال حرارت پایا ، گرادیان دما مثلا در بعد ، x شیب پروفایل دما را نشان می دهد در نتیجه پروفایل دما در پایا به صورت خط است و این خط نزولی است.
برای اینکه از حل تحلیلی معادلات انتقال حرارت بتوانیم استفاده کنیم باید برخی پارامترهای بدون بُعُد را قبل از حل مسئله بدست آوریم .
دمای بدون بعد – زمان بدون بعد – موقعیت بدون بعد – عدد بیوت Biot دمای بدون بُُعد )کسر دمایی()TR( )Temperature Ratio(: دمایی که انتقال نیافته
مثلا تخم مرغی که با دمای 5 درجه ، داخل آب 166 درجه وارد می کنیم ، انتقال حرارت ناپایا انجام می شود و دمای مرکز آن افزایش پیدا می کند.
دمایی که بعد از مدتی میگیردTi =5 Tm = 100 T=
هرچه می گذرد T به دمای محیط Tm نزدیک تر می شود ولی به آن نمی رسد زیرا همواره در حال دریافت گرما است مگر اینکه محیط دمای خود را از دست بدهد مثلا در مثال بالا از 166 به 46 برسد که T با آن برابر شود.
اگر نسبت دما یا TR را از 1 کم کنیم و در 177 ضرب کنیم درصد انتقال حرارت بدست می آید.
زمان بدون بعد )عدد فوریه()زمان انتقال حرارت(0F: زمان بر حسب ثانیه ضریب نفوذیعنی بعد از گذشت مثلا 17 دقیقه چه مقدار گرما انتقال پیدا کرده.
بعد مشخصه 2m
بُُعد مشخصه)موقعیت بدون بُُعد( : می تواند به جای x هر چیزی مانند y,z,r و غیره باشد.
حداکثر مسافتی که حرارت می تواند در جسم طی کند موقعیت بدون بعد ) از قسمتی که حرارت وارد نمی شود( جسمQ Slab
در شکل روبرو جسم از بالا و پایین در حال گرم شدن است
پس 0x برابر با نصف L است و x x برابر با فاصله مرکز تا نقطه L
ای که می خواهیم دما را در آن نقطه تعیین کنیم.
• اگر گرما از یک سمت وارد شود در نتیجه 0x برابر Q L می شود.
در کُُره یا استوانه بعد مشخصه ، شعاع است.
اگر حرارت در استوانه از سمت قائده)ارتفاع(وارد شود
hیاLجسم را همان Slab در نظر می گیریم. x
عدد بیوت یا بایوت Bi( Biot Number(:
این عدد نشان دهنده نسبت مقاومت جزوه انتقال جرم و حرارت داخلی نسبت به مقاومت حرارتی خارجی است.
???????? ?????? ?????????? مقاومت حرارتی داخلی
=مقاومتحرارتیخارجی
با توجه به رابطه صفحه قبل : در محیط سیال یا واسطه ، مقاومت جابجایی Convection ایجاد می شودو در جسم جامد ، مقاومت هدایتی Conduction ایجاد می شود که عامل محدود کننده در سرعت
در بیوت های بالا یا زیاد ) بیشتر از 47( ، مقاومت خارجی بسیار ناچیز است. در نتیجه سرعت
انتقال حرارت بین سطح جامد و توده سیال بسیار افزایش می یابد ، در چنین زمانی ، دمای سطح جسم به سرعت به دمای توده سیال نزدیک می شود ، بنابراین سیال یا مکانیسم جابجایی ، عامل محدود کننده انتقال حرارت نخواهد بود.
در بیوت های خیلی کم)کمتر از 7.1( مقاومت داخلی یا مقاومت هدایتی بسیار ناچیز است و انتقال حرارت بین سطح و مرکز جسم به سرعت انجام می شود ، به طوریکه در هر زمان ، نقاط مختلف جسم با هم ، هم دما می شوند بنابراین در چنین جسمی ، گرادیان دما نسبت به بُعُد صفر می شود .
برای نشان دادن رابطه دما و زمان در بیوت های کمتر از 6.1 بایستی از رابطه زیر استفاده کرد زیرا طبق گفتههای قبلی ، در بیوت های کمتر از 6.1 ، دما ، در جسم تنها تابعی از زمان است و به موقعیت بستگی ندارد به همین دلیل باید رابطه ای پیدا کنیم که زمان و مکان را نشان دهد:
دما از Ti به T می رسد و جسم در مایعی با دمای Tm جزوه موازنه جرم و انرژی گرفته و دمای جسم در حال زیاد شدن است ، موازنه
q با مکانیسم هدایت وارد جسم می شود در نتیجه رابطه به صورت زیر می شود
انتقال حرارت
رابطه بالا برای پیش بینی پیشینه دمایی ، زمانی که Biot کمتر از 7.1 است می توان استفاده کرد.
اگر فاز جامد را خیلی ریز کنیم )فقط فاز مایع باقی میماند و جامد بسیار ریز می شود ( عدد Biot به کمتر از 6.1 میرسد . به مواد غذایی که خوب همزده می شوند Well mix می گویند.
مثال صفحه 124 PDF :
مثال صفحه 165 :
مسئله برای Biot بالای 96 است چون دمای سطحی از استیک که بر روی سطحی داغ قرار گرفته است ، بلافاصله به دمای سطح داغ می رسد و در این دما باقی می ماند بنابراین می توان در نظر گرفت که مقاومت خارجی وجود ندارد . بنابراین برای حل اینگونه معادلات )بیوت جزوه انتقال جرم و حرارت از 96( بایستی به جدول 16.1 ص162 قسمت معادلات حل شده برای بیوت بالاتر از 96 مراجعه کرد.
1( local الف( a برای استوانه و Slab ب( b برای کُُره 2( mean
در فرمول صفحه قبل Fo دارای متغیر t است.
در رابطه ابتدا n=0 قرار می دهیم و فرمول را محاسبه می کنیم که اگر F0 بیشتر از 6.2 باشد ، همان جمله اول یعنی n=0 دقیق است و نیاز به محاسبه بقیه مقادیر n نیست.
زمانی که گرما از یک سمت وارد می شود 0x از سمتی که گرما وارد نمی شود تاجایی که گرما نفوذ میکند .
مثال 17.5 صفحه 127 :
شیر تغلیظ شده در یک قوطی با قطر 7.5cm و ارتفاع 9.5cm در حال استریل شدن )استریل شدن در بستر( می باشد .زمان مورد نیاز برای اینکه دمای شیر از℃ 95 به ℃115برسد .
a( قوطی به گونه ای دوران دارد که می توان دمای همه نقاط را یکسان فرض کرد .)بیوت کمتر از 6.1 می تواند رخ دهد(
تعیین u)ضریب کلی انتقال حرارت( به روش تجربی و با استفاده از نتایج آزمایشگاهی در شرایط بیوت کمتر از 7.1 : با استفاده از تکنیک regression
بعد از بدست آوردن پروفایل دما با روش تجربی ، سپس رگرسیون خطی می گیریم)به دلیل اینکه نقاط بدست
آمده روی یک خط نیستند پس نیاز به رگرسیون داریم(و شیب خط) a( را بدست می آوریم که این شیب خط سپس u را بدست می آوریم ومورد برسی قرار می دهیم.
نکته : در رگرسیون هرچه ضریب تبدیل) R-Square , R2( به 1 نزدیک تر باشد یعنی روند خطی تر است و نقاط پراکندگی کمتری دارند . و R2 حداقل باید بالا 6.46 باشد که کمتر از این مقدار نشان دهنده این است که روند خطی نیست و غیر قابل اعتماد است.
مثال 17.10 صفحه 147
سیب زمینی با قطر 5cm 1( زمان لازم برای اینکه مرکز جزوه انتقال جرم و حرارت زمینی به 54 برسد 2( میانگین دما در کل ماده زمانی که دمای مرکز به 54 برسد 3( به نظر شما زمان لازم برای سرمایش ، با قطر متناسب
از معادله حل شده برای Biot بیشتر از 47 در جدول 17.1 ص 172 بخش local قسمت c استفاده می کنیم.
نکته : اگر این نمونه در آبی که در حال جوش نبود قرار می گرفت بایستی معادله را برای بیوت بین 96 و 6.1 بنویسیم طبق جدول 16.1 .
نکته : اگر سیستم گرمایشی تحت فشار باشد)مثلا 2 اتمسفر( ، بایستی دمای جوش آب در آن فشار را استفاده کنیم .
،
سپس با جایگذاری اعداد در معادله ،Fo را بدست می آوریم و با استفاده ازاطلاعات مسئله α را محاسبه می کنیم و t را محاسبه می کنیم توسط فرمول Fo .
برای بدست آوردن میانگین دما بایستی از قسمت mean Temperature صفحه 172 بخش C ، Taverage یا Ta را بدست آوریم.
سینتیک یا کینتیک واکنش های تجزیه ای) decaying Reaction( :
در چنین واکنش هایی با گذشت زمان غلظت یک ماده به تدریج کاهش می یابد که اثر آن می جزوه انتقال جرم و حرارت کاهش پارامترهای فرآیند باشد )کاهش غلظت مواد مغذی در طی زمان در فرآیند حرارتی یا کاهش کیفیت یک محصول در طی نگهداری در انبار یا بسته(.
سینتیک یعنی برسی سرعت انجام واکنش ها و اثر مخرب فرآیند ها.
C = غلظت معادله کلی سینتیک
برای M.O ها بایستی تعداد آنها را به عنوان C قرار واکنش های تجزیه می دهیم K = ثابت سرعت واکنش) reaction constant rate(
برای پارامتر هایی مثل رنگ ، ابتدا باید آنها را به یک که به شدت به دما وابسته ست.
کمیت تبدیل کنیم سپس مورد استفاده قرار دهیم.
اگر n=0 قرار دهیم معادله درجه صفر Zero order خواهد شد در نتیجه سرعت تخریب با K برابر می شود و
واکنش ثابت است. dcdt K Cn - dcdt K dcdt K-با گذشت زمان میزان غلظت کاهش پیدا می کند و منفی ابتدای جمله برای مثبت کردن معادله است.
معادله واکنش درجه صفر خطی است در نتیجه نمودار آن هم به صورت خطی می باشد . سرعت واکنش در تمام مدت ثابت است )مثلا در هر 5 یا 16 دقیقه مقدار مشخصی)مثلا 1ppm( از غلظت یک ماده کاسته شود.
در این نوع واکنش ، رابطه بین غلظت و زمان به صورت خطی است و ثابت سرعت واکنش را می توان از روی شیب
نمودار بدست آورد.
: )First Order(1 واکنش درجه
در این نوع واکنش ها ، سرعت واکنش علاوه بر K به C )غلظت( هم بستگی دارد و سرعت واکنش در همه زمان ها یکسان نبوده و به خاطر رفتار نمایی exp ، در زمان های آغازین، سرعت از بین رفتن یا کاهش بیشتر است و هرچه به انتهای واکنش نزدیک می شویم ، تغییرات غلظت یا سرعت واکنش کمتر می شود زیرا در یک واکنش درجه 1 ، سرعت واکنش به غلظت نیز وابسته است.
نمودار این واکنش به صورت غیر خطی است .
در ابتدا به دلیل غلظت بالا، شیب نمودار زیاد است که با مرور زمان ، غلظت و سرعت و شیب نیز کاهش پیدا می کنند.
در یک واکنش درجه 1 ، رابطه بین غلظت و زمان ، غیر خطی است در حالی که رابطه بین لگاریتم طبیعی غلظت یا lnC و t زمان به صورت خطی می شود ، بنابراین اگر از غلظت های اندازه گیری شده در زمان های مختلف لگاریتم طبیعی) ln( بگیریم و آن را در برابر زمان رسم کنیم خطی نزولی بدست می آید که شیب این خط ، ثابت سرعت واکنش) K( خواهد بود. y a lnCاین کار را برای بدست آوردن K انجام lnC lnbC0 K tx
می دهیم.
تعیین درجه واکنش:
برای این کار ، ابتدا بین غلظت و زمان رگرسیون خطی می گیریم ، اگر R2 )ضریب تعیین( بیشتر از 7.47 باشد )یعنی به احتمال بیشتر از 46 % رابطه بین C و t خطی است( نشان دهنده خطی بودن رابطه می باشد و چنین واکنشی درجه 7 محسوب می شود.
حال اگر 2R کمتر از 6.46 باشد باید در مراحل بعد ، از غلظت های اندازه گیری شده ، لگاریتم طبیعی بگیریم و سپس بین lnC و t رگرسیون خطی بگیریم ، اگر 2R بیشتر از 6.46 باشد ، واکنش درجه 1 است و اگر کمتر از 6.46 باشد سینتیک واکنش ممکن است درجه 2 یا غیره باشد.
در فرآیند های صنایع غذایی اکثر واکنش ها از سینتیک درجه 1 پیروی می کنند و بخشی هم درجه صفر محسوب می شوند مثلا )از بین رفتن M.O ها در اثر حرارت و همچنین تخریب اکثر ترکیبات مغذی درجه 1 محسوب می شوند(.
زمان نیمه عمر) ( half time (t( :
در اکسل برای بدست آوردن معادله خط رگرسیون بایستی روی یک نقطه از نمودار کلیک راست کرده و از منوی باز شده گزینه Add trend line را کلیک می کنیم
برای تعیین D ، ابتدا باید نمونه حاوی M.O مشخصی ، در یک دمای ثابت قرار داده شود و با گذشت زمان تعداد M.O های باقی مانده شمارش گردد سپس در یک نمودار log مقدار باقی مانده در برابر زمان رسم شود ، اگر بین logN و t ، رگرسیون خطی بگیریم و 2R بیشتر از 46 باشد ، از روی شیب خط رگرسیون می توان Dvalue را بدست آورد . .
Dvalue و K به شدت به دما وابسته اند و DT وKT رابطه عکس جزوه انتقال جرم و حرارت. با افزایش دما طبق قانون آرنیوس ، ثابت واکنش از بین رفتن M.O ها ، افزایش می یابد و در نتیجه Dvalue کاهش می یابد .
واحد Dvalue = دقیقه یا ثانیه . واحد K =
اگر منحنی بقا برای یک M.O مشخص در دماهای مختلف رسم شود ، نمودار هایی با شیب های متفاوت بدست می آید که هرچه قدر دما بیشتر شود شیب نمودار بقا نیز بیشتر می شود در نتیجه سرعت از بین رفتن M.O )K(بیشتر می شود در نتیجه Dvalue کاهش می یابد.
اگر Dvalue های بدست آمده در دماهای مختلف در نمودار دیگری قرار گیرند ، نمودار مرگ حرارتی یا نمودار دما – زمان )Zvalue( بدست می آید که در این نمودار log Dvalue در برابر دما رسم شده است که برای تعیین Zvalue بین log Dvalue و T ، رگرسیون خطی می گیریم که اگر 2R بیشتر از 46 % شود ، شیب خط رگرسیون را 1 قرار می دهیم و Zvalue بدست می آید.
Dvalue = تعداد – زمان Zvalue = دما – زمان : معادل یک اختلاف دما) T∆( است به طوری که اگر دمای فرآیند حرارتی را به اندازه Z تغییر دهیم ، زمان لازم یک سیکل لگاریتمی تغییر کند . مثلا اگر دمای فرآیند حرارتی به اندازه Z افزایش یابد ، زمان باید یک سیکل لگاریتمی کاهش یابد) Dvalue ، 1 10 حالت قبل می شود(. و اگر دما به اندازه Z کاهش یابد ، زمان یک سیکل لگاریتمی افزایش می یابد) Dv ، 16 برابر حالت اول می شود(.
زمانی که log D یا log N در محور y ها قرار بگیرد ، نمودار بدست آمده خطی می شود ولی اگر N یا )( ، :
:
℃℉)(: -℉؟
:
: ؟
:
) ( ؟
?
فهرست مطالب